Con questo articolo comincio una serie di collegamenti all’interno e all’esterno del sito, in modo da rendere più chiaro e completo l’argomento.
La celiachia o morbo celiaco o sprue celiaca è un’enteropatia (ossia una patologia a carico del sistema intestinale) determinata dalla risposta immunitaria nei confronti dell’intestino stesso, in seguito alla reazione contro il glutine, di cui parlerò in maniera approfondita in seguito.
La Non Celiac Gluten Sensitivity (NCGS) o Sensibilità al glutine è una condizione clinica che interessa l’intestino, in seguito all’ingestione del glutine, descritta per la prima volta nel 1978 da Ellis e Linaker e poi nuovamente nel 1980 da Cooper. Tuttavia, perché ci tengo a precisare i nomi e le date? * di solito non lo faccio mai perché nel mio sito mi rivolgo ai pazienti e non ai colleghi* Perché solo nel 2012 è stata inserita nello spettro dei disordini determinati e correlati al glutine, insieme alla celiachia (Celiac Disease o CD) e all’allergia al grano (WA), motivo per cui è spesso poco conosciuta e tante persone che hanno sintomi simili alla celiachia non hanno una diagnosi certa!
Entrambe le condizioni hanno in comune la risposta verso il glutine, leggi qui, e come conseguenza un’alterazione nella permeabilità instestinale (che diventa un vero e proprio “colabrodo”, ne ho parlato anche qui e qui).
Per cui la sintomatologia è molto simile:
- a livello intestinale con dolore addominale, gonfiore, alterazioni dell’alvo ;
- a livello extra-intestinale con stanchezza cronica, mal di testa, annebbiamento, dolori muscolari e articolari, eczema o rush cutaneo, depressione, anemia.

Quali sono le differenze?
La differenza tra la celiachia e la gluten sensitivity è determinata principalmente dalla reazione immunitaria (di cui ho parlato dettagliatamente qui e qui) in quanto:
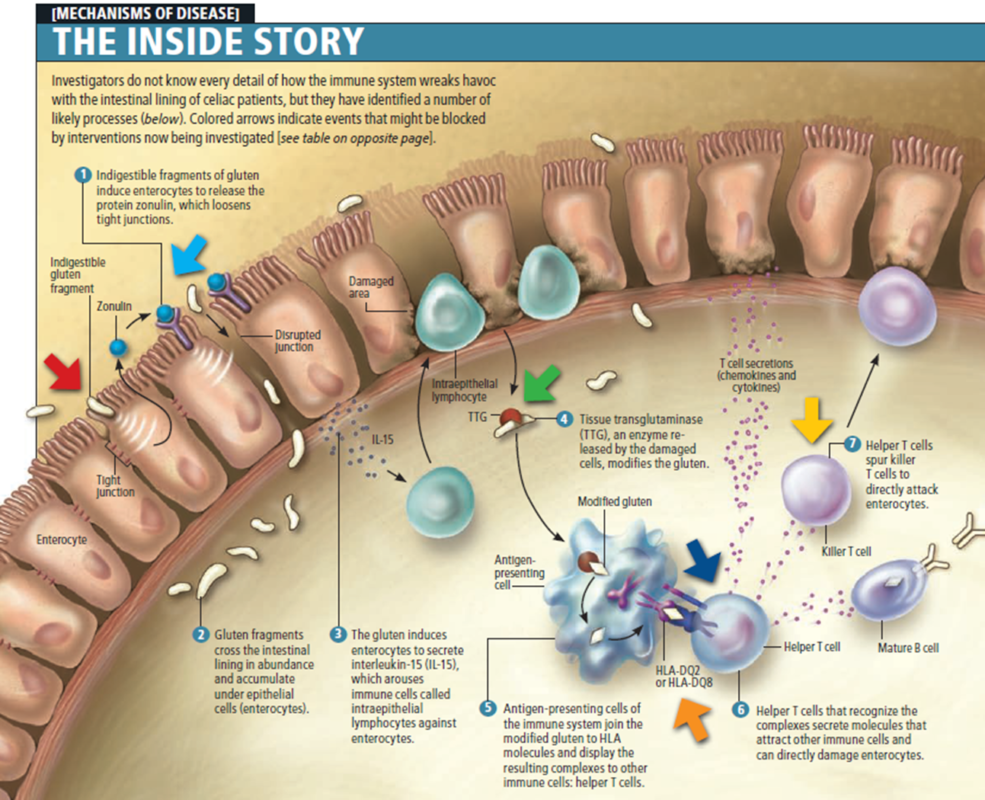
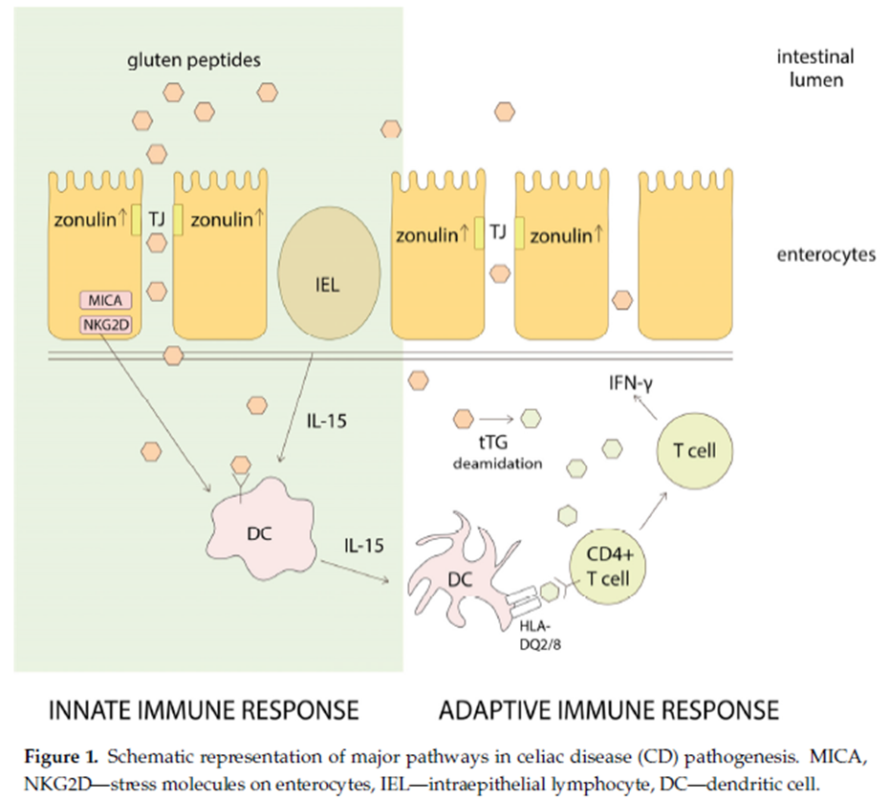
Nella celiachia la risposta immunitaria è di tipo adattativo ossia si ha l’attivazione di specifici linfociti, detti CD8+, che diventano citotossici ossia in grado di distruggere gli enterociti (le cellule intestinali) segnalate da una proteina presente sulla loro superficie, quasi come fosse una bandierina di riconoscimento, detta MIC-A simile alla HLA di classe I espressa in risposta allo stress. L’attivazione di tali linfociti avviene attraverso specifiche componenti del glutine, ottenute in seguito alla sua digestione e riconosciuti come estranei da parte di HLA DQ2 o HLA-DQ8, questi ultimi però devono essere mutati per determinare una risposta immunitaria (mentre in un soggetto “non mutato”, e quindi non predisposto, tale reazione non avviene) presentando l’elemento riconosciuto come estraneo (ossia pezzettini del glutine) ad altri linfociti (armi del sistema immunitario) detti CD4+ in grado di determinare l’aumento dei linfociti intraepiteliali, l’allungamento delle cripte e l’atrofia villosa ossia si ha un’alterazione locale delle strutture che compongono la barriera intestinale (ricca di cripte e villi, che costituiscono una difesa e una barriera tra ciò che arriva dall’alimentazione e il circolo sanguigno). Inizia cosi una cascata di risposte del sistema immunitario che producono anticorpi IgG e IgA contro:
- la gliadina deaminata (AGA)
- la transglutaminasi tissutale (tTG)
- l’endomisio (EMA)
Fasano 2009, Surprise from Celiac Disease
Nella Non Celiac Gluten Sensitivity (NCGS) o Sensibilità al glutine la risposta immunitaria, che determina la sintomatologia intestinale, è innata, e non adattativa come nel caso della celiachia, per cui non abbiamo la presenza di anticorpi nel sangue. Tuttavia il legame della gliadina (la porzione reattiva del glutine) al recettore della mucosa intestinale CXCR3, determina il rilascio della zonulina, come se il legame tra la gliadina e il recettore fosse un pulsante di rilascio di questa molecola che regola e garantisce la permeabilità intestinale, determinando il passaggio delle sostanze provenienti dall’alimentazione (sia quelle importanti che non) dal lume intestinale alla lamina propria, scatenando la risposta immunitaria innata.
Come viene effettuata la diagnosi?
Come sempre per le parti che non sono di mia competenza chiedo la collaborazione di esperti e riporto di seguito l’intervento del Dott. Dimonte Salvatore, direttore del laboratorio BioMolecularLab, a riguardo:
Gli esami di laboratorio sono fondamentali per l’inquadramento della malattia celiaca e spesso sono in grado di individuare soggetti celiaci asintomatici o con segni clinici subdoli e di non facile interpretazione.
Alla luce di quella che è la fisiopatologia ossia le conseguenze della patologia a livello fisiologico, la diagnosi viene effettuata attraverso due indagini:
- Test invasivo che si basa sul prelievo o biopsia della mucosa del duodeno (la seconda porzione del duodeno e del digiuno prossimale, leggi qui, sono le più esposte alla risposta immunitaria contro il glutine), in modo da valutare la presenza di un aumentato numero dei linfociti CD8+ intraepiteliali (linfocitosi intraepiteliale), la proliferazione delle cripte con loro rispettivo allungamento e atrofia dei villi.
- Test meno invasivi rispetto alla biopsia che si effettuano mediante test sierologici volti ad identificare la presenza di anticorpi anti IgA o IgG della gliadina deaminata, anticorpi IgA della transglutaminasi tissutale e gli anticorpi antiendomisio.
Nel 1997 l‘enzima transglutaminasi tissutale (tTG) è stato identificato quale principale se non unico bersaglio degli autoanticorpi presenti nel siero dei soggetti celiaci. L’enzima agisce deamidando la gliadina che, così modificata e associata agli antigeni del complesso maggiore di istocompatibilità di classe II (HLA II) DQ2 o DQ8, viene presentata ai linfociti T della lamina propria intestinale.
L’anti-tTG è l’anticorpo più comunemente usato poiché, oltre alla sua elevata sensibilità e specificità (entrambe circa il 95%).
Gli anticorpi anti-gliadina (AGA) sono stati il primo marcatore sierologico a essere utilizzato nella pratica clinica.
La dimostrazione che i soggetti affetti da malattia celiaca esprimono selettivamente gli antigeni HLA di classe II DQ2 o DQ8 ha permesso di introdurre questa indagine genetica nella pratica clinica.
La molecola DQ2 è un eterodimero formato da una catena α e una catena β, è situata sulla superficie delle cellule coinvolte nella risposta immune (linfociti B e macrofagi).
L’aplotipo o la combinazione di varianti del DQ2 è presente nel 90-95% dei pazienti celiaci e la percentuale residua dei pazienti celiaci DQ2 negativi porta l’aplotipo DQ8.
L’identificazione dell’aplotipo associato a celiachia non deve essere considerato un test di conferma, ma piuttosto un esame a completamento del quadro diagnostico in alcune situazioni particolari e deve quindi essere utilizzato come marcatore di esclusione di malattia.
N.B. Questi test devono essere effettuati durante l’assunzione del glutine per evitare falsi negativi!
La celiachia può presentarsi in due forme differenti a seconda dei risultati dei test diagnostici:
- Celiachia silente, con test sierologici negativi e atrofia dei villi ma senza sintomi (motivo per cui è detta silente, e su cui è utile indagare in caso di ipofertilità)
- Celiachia latente, con test sierologici positivi e atrofia dei villi.
Nella Non Celiac Gluten Sensitivity (NCGS) o Sensibilità al glutine essendoci una risposta immunitaria innata, quindi senza la produzione di anticorpi specifici, non troveremo una positività dei test sierologici ma la sintomatologia sarà la stessa e l’unica evidenza della presenza di un problema ossia il malassorbimento intestinale!
Cosa le accomuna? La sintomatologia
La sintomatologia presenta alla base il malassorbimento intestinale, ossia la funzione di barriera tra l’interno e l’esterno, tra il lume intestinale e il circolo sanguigno, svolta dall’intestino viene a mancare. L’intestino diventa un vero e proprio colabrodo, per risposte immunitarie differenti (innata e adattativa) ma che portano ad un esito comune e per fortuna reversibile.
In entrambe la sintomatologia si manifesta a livello intestinale con:
- Diarrea cronica;
- Meteorismo, dolori addominali e movimenti irregolari dell’intestino;
- Gonfiore o distensione addominale;
- Anemia e ferro basso (in quanto è a livello intestinale che avviene maggior assorbimento);
- Stanchezza;
- Affaticamento cronico;
- Emicrania;

Ma possono anche presentarsi sintomi extra-intestinali, in particolare nella celiachia:
- Artrite o dolori alle articolazioni;
- Stomatite aftosa o afte ricorrenti;
- Anemia sideropenica;
- Pubertà ritardata e bassa statura;
- Infertilità.
Infine rientra come conseguenza comune anche l’infertilità, in quanto il malassorbimento presente alla base delle due, sia per la celiachia che per la gluten sensitivity, impedisce l’assorbimento del ferro (essenziale per la fertilità), altera la produzione del complesso delle Vitamine B (in particolare la Vitamina B12 prodotta dai ceppi batterici intestinali, che risultano alterati nella composizione del microbiota intestinale), altera l’assorbimento dell’acido folico e i livelli della Vitamina D.
Qual è il trattamento e la terapia?
Per entrambi un’alimentazione senza glutine, ma sottolineo non solo a base di prodotti gluten free industriali, come ho scritto qui in relazione ai carboidrati. Inoltre è importante fare diagnosi molto prima in modo da garantire il ritorno ad una condizione “normale”, e non del tutto alterata, in quanto pur essendo condizioni reversibili, portano a conseguenze importanti se trascurate. Motivo per cui è importante non sottovalutare nessun sintomo, anche in fase pre o adolescenziale, e nonostante ci siano test diagnostici con risultato negativo, se la sintomatologia persiste!
